Вакцинами называют антигенные препараты, употребляемые для иммунизации людей и животных с целью создания у них искусственного активного иммунитета. Вакцины большей частью применяют для профилактики и лишь немногими вакцинами пользуются для лечения инфекционных заболеваний (дизентерия, бруцеллез).
Бактерийные, риккетсиозные и вирусные вакцины изготовляют институты вакцин и сывороток. Вакцины могут быть приготовлены из убитых или живых ослабленных микробов, а в ряде случаев из соматических антигенов микробной клетки (химические вакцины).
Убитые вакцины представляют собой взвесь инактивированных микробов в изотоническом растворе хлорида натрия (корпускулярная вакцина). Для инактивирования микробной взвеси пользуются нагреванием (до 56—58°С) или действием химических веществ (этиловый спирт, формалин и др.). Соответственно получают гретые, формалиновые, спиртовые и другие вакцины.
 Приготовление убитой (корпускулярной) бактерийной вакцины состоит из нескольких этапов. Приготовление убитой (корпускулярной) бактерийной вакцины состоит из нескольких этапов.
1. Подбор вакцинных штаммов. Для приготовления убитой вакцины отбирают несколько наиболее вирулентных и полноценных в антигенном отношении штаммов.
2. Массовое выращивание культур и приготовление взвесей. Выращивание культур производят в жидкой питательной среде с аэрированием в специальных котлах. В отдельных случаях культивирование производят на плотных средах, разлитых в плоские бутыли — матрацы. Культуры, выращенные на плотных средах, смывают стерильным изотоническим раствором хлорида натрия.
3. Инактивирование вакцины путем нагревания или добавления химических веществ (при приготовлении спиртовых вакцин используют 97° этиловый спирт, формалин добавляют в количествах от 0,5 до 1%).
4. Титрование вакцины (стандартизация). Готовая вакцина должна содержать определенное количество микробных тел в 1 мл. Титр вакцины выражается числом микробных тел (миллионы, миллиарды) в 1 мл.
5. Сведение вакцины, т. е. соединение вакцин, приготовленных из различных видов или типов микробов. К готовой вакцине добавляют консервант (фенол 0,25%, мертиолат в соотношении 1:10 000 и др). Готовую вакцину разливают в стерильные ампулы или флаконы.
Для создания иммунитета к нескольким инфекциям пользуются ассоциированными вакцинами. В зависимости от числа входящих в вакцину микробных видов их называют моно-, ди-, три- и т. д. или поливакцинами. Например, тифопаратифозная дивакцина состоит из убитых путем нагревания возбудителей брюшного тифа и паратифа В.
Химические вакцины приготовляют из соматических антигенов (полисахаридо-полипептидо-липоидных комплексов), извлеченных из бактериальной клетки различными путями. Примером химической вакцины может служить тифопаратифозно-столбнячная вакцина (TABte), состоящая из О-антигенов брюшнотифозных и паратифозных А- и В-бактерий и столбнячного анатоксина. Все антигены сорбированы на гидроокиси алюминия.
Вирусные и риккетсиозные вакцины приготовляют из культур, выращенных на курином эмбрионе, культуре ткани или в организме животного.
Наиболее эффективными препаратами для создания искусственного иммунитета являются живые вакцины. Для приготовления живых вакцин необходимо располагать вакцинными штаммами (мутантами), обладающими стойко сниженной вирулентностью, но сохранившими иммуногенные свойства. С трудом удается получить вакцинные штаммы, и этим объясняется то, что, несмотря на большую эффективность живых вакцин, они еще не вытеснили менее эффективные убитые вакцины.
Значительные трудности имеются и на пути стабилизации необходимых свойств вакцинных штаммов, т. е. того состояния культуры, в котором она обладает максимальными иммуногенными свойствами и сниженной вирулентностью. Для целей стабилизации вакцинных штаммов, а также для сохранения жизнеспособности готовых живых вакцин пользуются методом лиофилизации. Этот метод консервирования живых микробов заключается в высушивании под вакуумом предварительно замороженного препарата или культуры.
Живые вакцины изготовляют из вакцинных штаммов бактерий (бруцеллезная, туберкулезная, сибиреязвенная и др.) и вирусов (оспенная, полиомиелитная и др.). Для получения живых бактериальных вакцин вакцинные штаммы выращивают на соответствующих питательных средах, а при приготовлении вирусных вакцин вакцинный штамм размножают в культуре ткани, на курином эмбрионе или в организме животного. Так, например, для получения противооспенной вакцины производят накожное заражение телок вирусом коровьей оспы и содержимое развившихся пустул используют для приготовления оспенной вакцины; вакцинные штаммы вируса полиомиелита размножают в культуре ткани почки зеленой мартышки и др.
Приведем примеры получения некоторых живых вакцин.
Противотуберкулезная вакцина БЦЖ (BCG). Вакцинный штамм BCG (бациллы Кальметта и Герена — Calmette и Guerin) получен французскими учеными Кальметтом и Гереном путем длительного культивирования вирулентного штамма микобактерий туберкулеза бычьего типа на картофельно-глицериновой среде с добавлением желчи. Культивирование продолжалось в течение 13 лет. За этот период было проведено 230 пассажей, в результате чего вирулентность культуры значительно снизилась. Для изготовления противотуберкулезной вакцины штамм БЦЖ выращивают на специальных средах в течение 20 дней. Приготовленную вакцину высушивают методом лиофилизации.
Антирабическая вакцина была получена Пастером. Вакцинный штамм для приготовления этой вакцины (virus fixe) был получен путем многочисленных пассажей (133 пассажа) вируса бешенства через организм кролика путем внутримозгового заражения. Это привело к сокращению инкубационного периода с 20 до 5—6 дней. В настоящее время вакцину готовят из мозга животных (овцы, сосунки белых крыс), зараженных фиксированным вирусом по методу Ферми. Вакцину выпускают в сухом виде.
Сибиреязвенная вакцина была также предложена Пастером. Путем культивирования сибиреязвенных бактерий при температуре 42,5°С были получены вакцинные штаммы различной степени пониженной вирулентности в зависимости от продолжительности культивирования. В связи с тем что при этой температуре сибиреязвенные бактерии теряли способность к спорообразованию, для закрепления полученных свойств их переводили в споровые формы путем культивирования при температуре 35°С.
Иной метод получения сибиреязвенной вакцины был использован советскими учеными — H. Н. Гинсбургом с соавторами. Пользуясь методом селекции, им удалось отобрать мутант сибиреязвенной палочки с ослабленной вирулентностью, потерявший способность образовывать капсулу (бескапсульный мутант). Этот мутант используется для приготовления сибиреязвенной вакцины (СТИ).
Вакцины выпускают в жидком и сухом виде. Жидкие вакцины представляют собой мутные жидкости, в которых при стоянии образуется осадок, легко разбивающийся при встряхивании.
Сухие вакцины изготовляют из микробных взвесей, высушивая их методом лиофилизации (высушивание из замороженного состояния под вакуумом). Сухие вакцины выпускают в запаянных ампулах. Они имеют вид белой или желтоватой плотной массы, хорошо растворимой в воде. Перед употреблением сухую вакцину растворяют стерильным изотоническим раствором хлорида натрия или дистиллированной водой с соблюдением всех правил асептики. Количество жидкости, добавляемой к сухой вакцине, должно быть указано в прилагаемом к вакцине наставлении.
Все вакцины проходят государственный контроль. Вакцины проверяют на стерильность (убитые вакцины) путем посева на питательные среды. Для проверки берут не менее трех образцов. Флаконы или ампулы вскрывают стерильно. При вскрытии ампулы следует накалить на пламени горелки ее горлышко, смочить его мокрым ватным тампоном (после чего стекло дает трещины) и легким ударом пинцета отколоть горлышко у пламени горелки. При посеве из флакона следует обжечь горлышко, извлечь пинцетом пробку, вновь обжечь горлышко и стерильной пипеткой набрать вакцину. Вакцину в объеме 0,5 мл сеют на следующие питательные среды: мясопептонный бульон, мясопептонный агар и среду Китта — Тароцци. Посевы выдерживают в термостате в течение 5—8 сут. Отсутствие помутнения на жидких средах и роста на агаре свидетельствует о стерильности вакцины. Проверку безвредности производят на мышах, которым подкожно водят 0,5 мл вакцины. Каждую вакцину испытывают не менее чем на трех животных. Мышей наблюдают в течение трех дней. Выживание животных свидетельствует о безвредности вакцины.
Густоту вакцины проверяют оптическим путем, используя стандарты, содержащие 5 и 10 единиц мутности, 1 мл испытуемой вакцины наливают в стандартную пробирку и затем добавляют в нее столько изотонического раствора хлорида натрия, чтобы степень мутности сравнялась с мутностью стандартной взвеси. Объем добавленного раствора хлорида натрия укажет, во сколько раз исследуемую взвесь пришлось развести, чтобы установить в ней мутность, соответствующую стандарту. Например, если к 1 мл вакцины потребовалось добавить 1,5 мл раствора хлорида натрия, чтобы мутность уровнять со стандартом в 10 единиц, следовательно, микробную взвесь пришлось развести в 27г раза и, таким образом, исследуемая вакцина содержала 2,5 млрд, микробных клеток в 1 мл.
Кроме того, проверяют бактериоскопическую чистоту препарата и иммуногенность. Для проверки иммуногенности производят иммунизацию мышей, после чего их заражают смертельной дозой соответствующей живой культуры. Процент выживших животных указывает на степень иммуногенности (60—80—100% выживаемости).
Готовые вакцины выпускают в ампулах или флаконах, снабженных этикетками. На этикетках должны быть указаны институт, изготовивший вакцину, название вакцины, серия, номер государственного контроля, срок годности и надпись «перед употреблением взбалтывать». В коробки с вакциной обязательно вкладывают наставление по применению данной вакцины.
Срок годности устанавливают для каждого вида вакцины отдельно при условии правильного хранения.
Сухие вакцины имеют большие сроки годности, чем жидкие. Так, например, сухая антирабическая вакцина имеет срок годности 2—3 года, жидкая — 5 мес. и т. д.
Признаки негодности вакцины: изменение нормального внешнего вида, изменение цвета, резкое помутнение или, наоборот, просветление, наличие плесени, посторонних частиц, комочков, не разбивающихся при встряхивании, нарушение целости ампулы, подтекание флакона, отсутствие этикетки. Сухая вакцина, не образующая при растворении равномерной взвеси, также не пригодна к употреблению.
Вакцины хранят в сухом, защищенном от света месте, при температуре, указанной в наставлении. Для большинства вакцин установлена температура хранения 2— 10°С.
Большинство вакцин вводят под кожу (вакцина против кишечных инфекций, антирабическая и др.), живые вакцины нередко вводят внутрикожно (вакцина БЦЖ) или накожно (оспенная, туляремийная и др.). Живую полиомиелитную вакцину применяют энтерально, а гриппозную — интраназально.
Убитые вакцины вводят 2—3 раза с интервалами 7— 10 дней. Живые вакцины, а также сорбированные препараты (химические вакцины, анатоксины) вводят, как правило, однократно. Адсорбция легко растворимых антигенов на индифферентных плохо растворимых соединениях (алюминиевые квасцы, фосфат кальция) способствует более длительному пребыванию антигена в организме и активирует синтез антител (адъювантное действие).
На практических занятиях студенты проводят контроль убитой вакцины.
Проверяют:
а) состав вакцины и срок годности;
б) изучают внешний вид вакцины: гомогенность, цвет, количество, этикетку, укупорку;
в) проверяют стерильность, стандарт и безвредность.
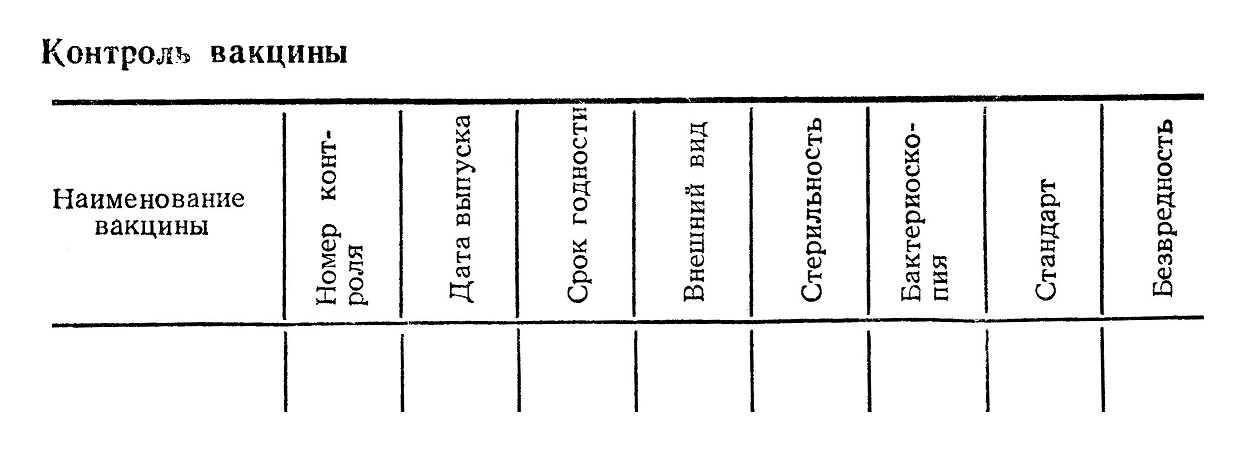
Результаты проведенного контроля оформляют в виде таблицы.
 Занятие 1-е. Вакцины и анатоксины. Вопросы для обсуждения. 1. Искусственный иммунитет, активный и пассивный. 2. Препараты для создания искусственного активного иммунитета: вакцины и анатоксины. 3. Виды вакцин: живые, убитые и химические. 4. Способы приготовления вакцин. 5. Анатоксины нативные и очищенные, их получение и титрован... Читать далее... |
|  Приготовление убитой (корпускулярной) бактерийной вакцины состоит из нескольких этапов.
Приготовление убитой (корпускулярной) бактерийной вакцины состоит из нескольких этапов.